公司中试厂房要开工,受限于空间无B级洁净区考虑使用无菌隔离器,隔离器需要在厂房完工前塞进去。公司处于初创阶段不想投入过多,隔离器选择时排除进口隔离器考虑国产的无菌检查隔离器。基于以上考虑对隔离器选型时更关注成本和时效性。
1无菌隔离器用户需求说明(URS)该怎么写?
用户需求说明是从网上下载一个还是向供应商要一个呢?
隔离器不同于其他定制仪器设备,需要从设计确认根据用户的使用目的进行个性化定制,为了考虑效率和质量稳定,定制时又不能有过多的灵活性,基本上就是在厂家提供的常用方案上进行调整和选择。因此这个用户需求要按照自己的需要进行书写。那如何进行这个URS的书写呢?怎么得出这个URS来?
1.1参考相关法规理清思路
1.1.1无菌检查隔离器相关法规
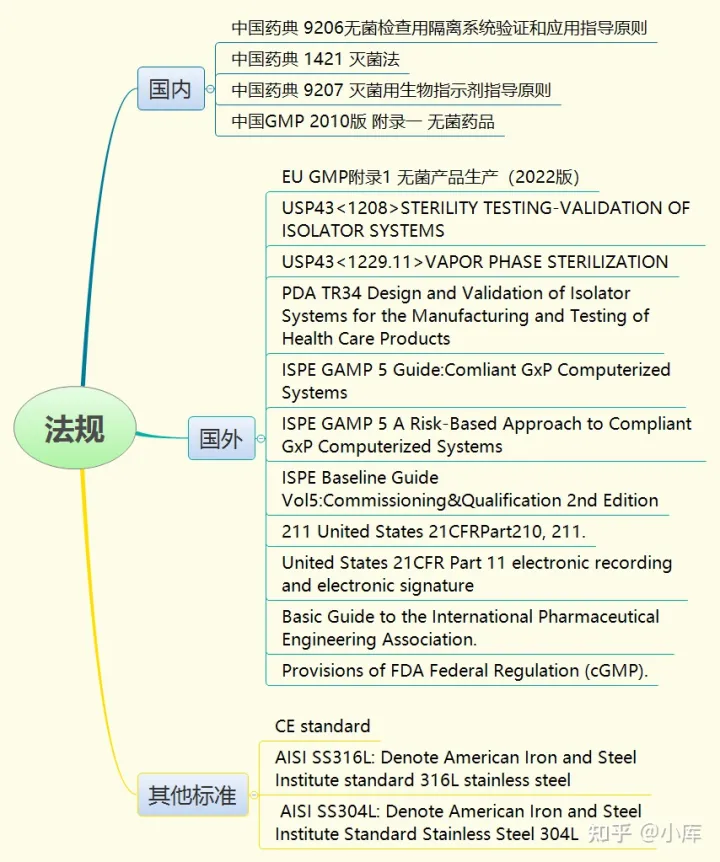
无菌隔离器的URS模板内容较多,如果不理清其思路难免会落入下乘。我个人理清思路的方法就是看法规,同时参考URS书写模板进行思路的书写,前者让我清楚无菌检查隔离器的个性要求,后者让我补缺补漏。URS书写模板像一个目录,后者是具体指导,结合自己的需求就可以写出自己需求的URS了。附上常见相关法规,特别提示建议着重关注中国药典9206、USP<1208>和PDA TR34。
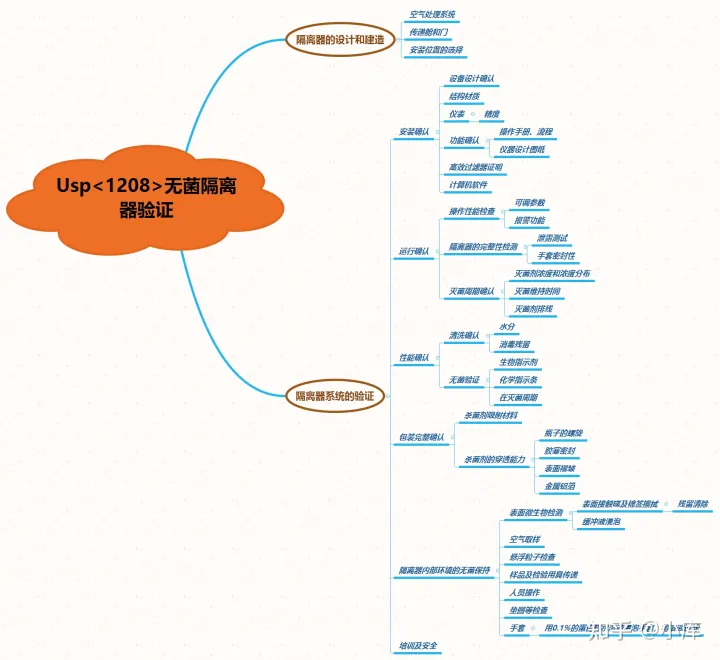
1.1.2USP<1208>无菌隔离器验证的相关内容
仪器的3Q验证实际上就是对用户需求的确认。从无菌检查隔离器验证的相关要求,我们可以逆推得出我们的需求额着重关注的内容。
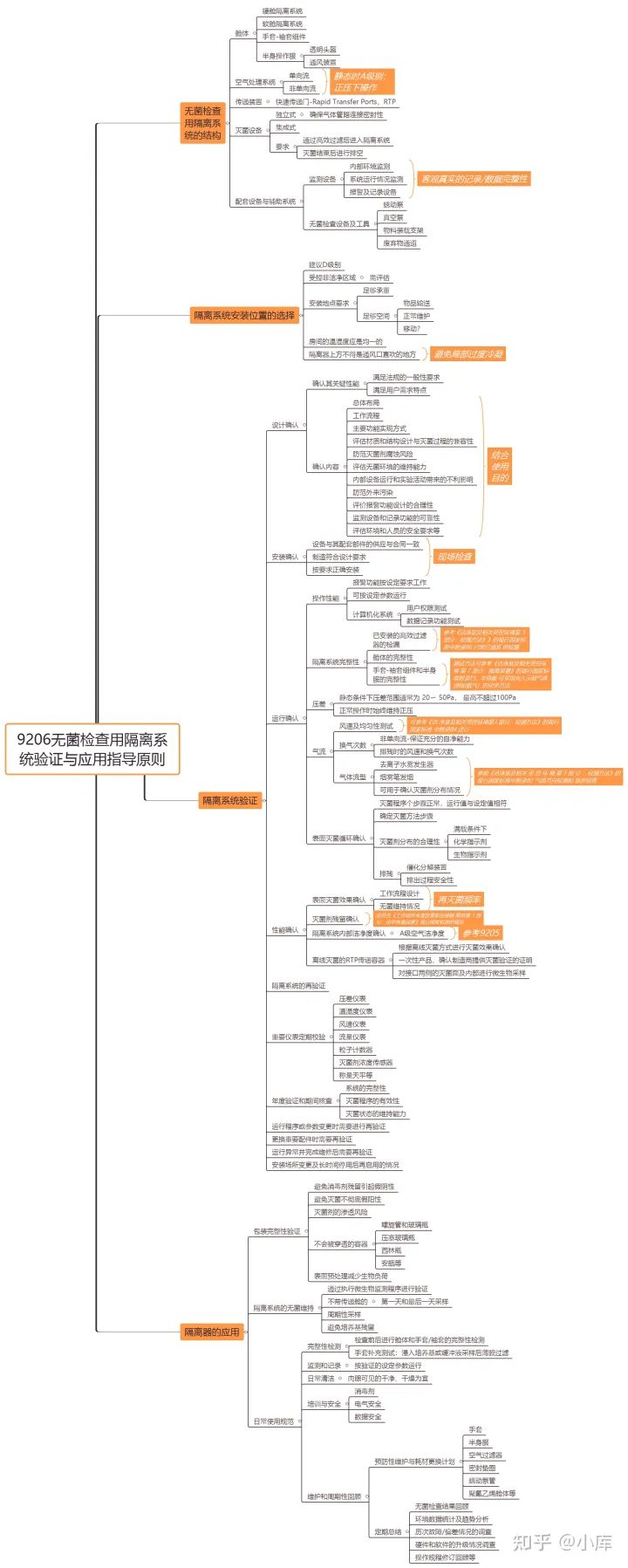
1.1.3 9206无菌检查用隔离系统验证与应用指导原则
9206无菌检查用隔离器验证与指导原则可以说是USP<1208>和PDA TR 34的集合体,通过学习9206基本可以梳理出所有关于无菌隔离器的基本需求。其中9206关于各测试项目的检测参考标准都进行了明确,这一点很不错。我们用户需求的框架可以参考9206关于隔离器结构和位置选择等下的内容展开,关于细节要求参考隔离器验证和应用的相关要求。
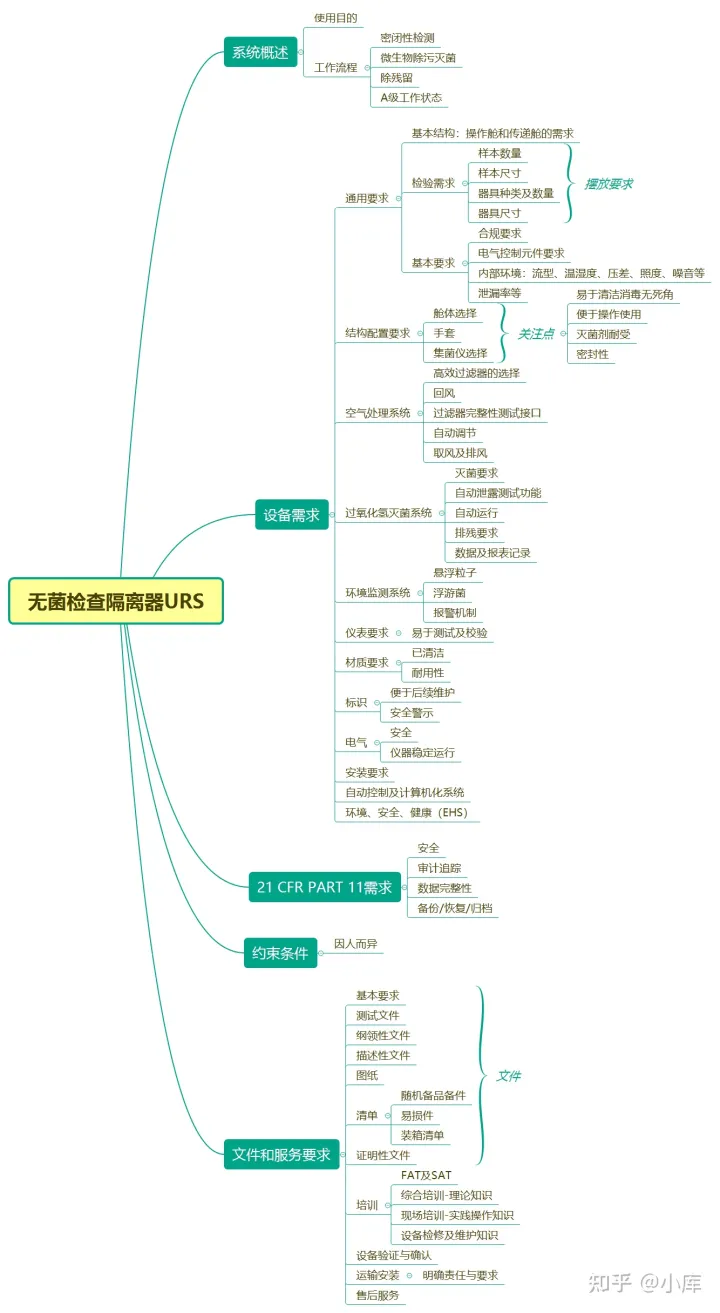
1.1.4隔离器用户需求草稿
前面法规梳理完,关于设备需求部分没问题了,我们还需要注意系统概述、数据完整及计算机化系统相关要求、文件和服务需求等。其中系统概述、数据完整及计算机化系统相关要求,这两部分内容没有特别的不同。关于文件和服务需求业务也无明显不同,但个人认为这两部分需求特别的关注和用心。我们可以在这一部分尽可能的维护我们自己的利益。文件是我们可以留下的证据,虽说我们不写供应商也会提供,但有些东西我们不要,到了执行层面就会出现遗漏或者偏差。因此后续审计会被查到的内容我们就要走心。关于服务,不用客气,此时客气了以后就没机会了。特别是明确责任和义务,不落在纸面上,别人做到了是情面,做不到你也无可奈何,毕竟和我们签合同的和做事的不是一个人。以下是个人梳理的用户需求草稿供参考。
1.2参考使用需求进行细节优化
对于检品多输液袋时就需要在操作舱舱体多加1-2个1横杆或悬挂小车,注意尽可能不要影响气体流型。如考虑采用杀孢子剂进行表面消毒,那么可以考虑不进行悬挂。
多于样品大小不同确定样品支架的孔径等,为确保过氧化氢实现对瓶底的消毒5mL西林瓶和100mL输液瓶的孔径不同等。对于大输液瓶,圆孔和长条孔区别不大,但对于小西林瓶则不同。总之不同的使用需求需要对细节进行优化,一定要注意尽可能不影响流型和表面消毒。过氧化氢不具备特别强的穿透能力,需要消毒的表面如不能做到消毒则需要采用补充方式。
2无菌隔离器设计确认时的考虑该部分主要是对隔离器配置选择时个人的考量,更多是个人主观意愿,此处有毒,自行决策,切勿随意模仿。
2.1要传递舱吗?
不要。原因如下:
1)作为研发企业我们没有特别大的样本量,我们不需要传递舱采确保使用面积。
2)隔离器灭菌前后我们会根据检查清单进行物品确认,不需要传递舱来应付意外情况,其次如果漏了还没检查出来,那么这个人及时有传递舱也要加班,何必呢,隔天做吧。
3)传递舱可以实现隔离器的连续使用。且不说灭菌维持时间验证,又不是24小时上班,持续运行产生的能耗和维持过程可能带来的污染风险都在告诉我们谨慎抉择。而且现在还可以预约灭菌的前提下,单操作舱是理智的选择。
4)然后吐槽一点,加传递舱验证的时候不是3+3的验证,首次应该是3(操作舱)+3(传递舱)+3(联合灭菌),此时选择操作舱就很香了。
5)考虑成本,在不是非常需要的情况下舍弃传递舱,毕竟我们要压缩成本。
6)然后强调一下,根据自己需求选择,有时候单操作舱还可以选择两面的,根据需求选择。
2.2关于单向流这一点很重要吗?
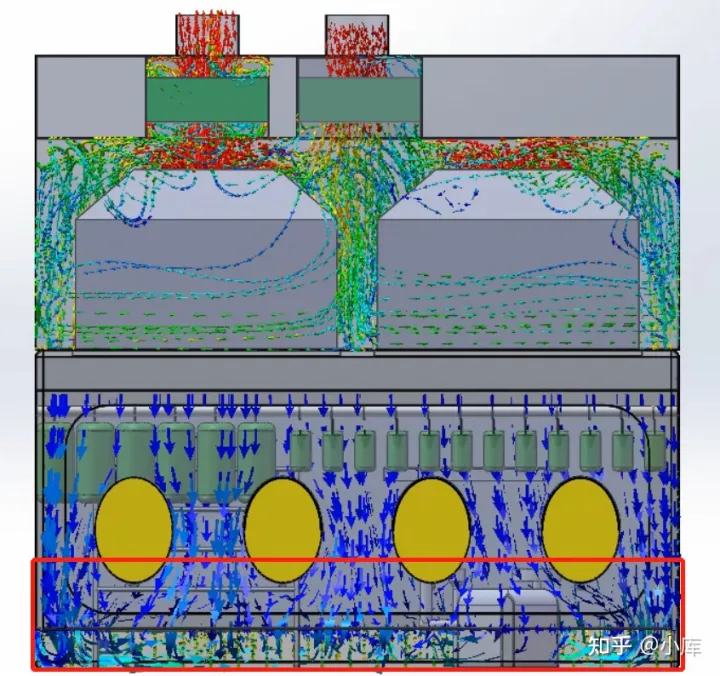
单向流相对于紊流更有优势,如果表面不能做到完全无菌或者存在阳性样本,那么紊流就存在交叉污染的可能。不过需要明确一点,单向流送风不一定是单向流,此时物品的布局摆放会引起局部紊流,因此在单向流送风基础上设计好舱体内物品摆放更重要。
无菌检查隔离器内部气体流型示意图(图片来源于网络,仅供学习交流用)
2.3过氧化氢干法灭菌和过氧化氢蒸汽灭菌该如何选择?
1)通常说的湿法是不进行除湿直接进行过氧化氢灭菌,而市面上的国产隔离器都是控制温湿度的,没有传统意义上的湿法灭菌,因此不存在干法和湿法的抉择。
2)其次对于干法不易腐蚀这一点,我们选用的材质都是耐过氧化氢腐蚀的,在使用频次不是特别高的情况下,干法的优势并不明显,其优势只是局限于理论上。
3)干法灭菌的不足在于对温湿度要求更为苛刻这一点对于处于洁净区,而且是封闭空间的无菌隔离器里面,这并不是什么不可接收的不足。
4)对于干法需要样本恢复一定温度这点,实际上过氧化氢灭菌均为微冷凝,温度过低都引起局部过度冷凝,因此这也不是干法的缺点。
5)至于对高效过滤器的影响很难说,都是道听途说,没有明确的要求。
6)过氧化氢浓度并不是过氧化氢灭菌的决定因素,关于两种方法的灭菌时间差异并无明确要求。综上,实际上过氧化氢干法灭菌和过氧化氢灭菌没有明显的区别,更多是仪器制造商的一个宣传策略。我们需要做的是如何做好选择后的应对策略。如:控制物品表面的水分、样本需恢复到室温等策略。
2.4集菌培养器可以选择国产的吗?
对于我们使用频次低,不计划进行国外申报的前提下,为了控制成本选择国产集菌仪了。虽然做了这样的选择,但是还是再担心国产集菌仪控制面板会不会耐受过氧化氢,并无其他担忧。
2.5过氧化氢探头该怎么选择?
现在主要是D和V两个厂家的过氧化氢探头。D的探头是电化学探头,其使用寿命相对短一些;其稳定性会好一些;分高低探头会增加计量成本;更换探头时需要进行隔离器灭菌的再验证。V探头容易受有机溶剂影响,因此舱体内不便使用乙醇等进行清洁消毒;其次探头的稳定性据说存疑;该探头寿命也是有限的,存在老化的情况,也需要定期的隔离器再验证。基于以上考虑,两种探头各有优缺点,选择后基于选择做出评估,制定自己的再验证策略即可。
2.6手套该怎么选择?
关于乳胶手套和其他材质手套来说,乳胶手套存在不耐臭氧的问题,但是乳胶手套便宜,如果进行臭氧灭菌时候将手套做好密封即可解决问题。为了便于操作,手套的材质影响并不大,手套的厚薄对操作影响更大。在保证密封性的前提下,选择尽量薄的手套为佳。
3其他鸡毛蒜皮的小事
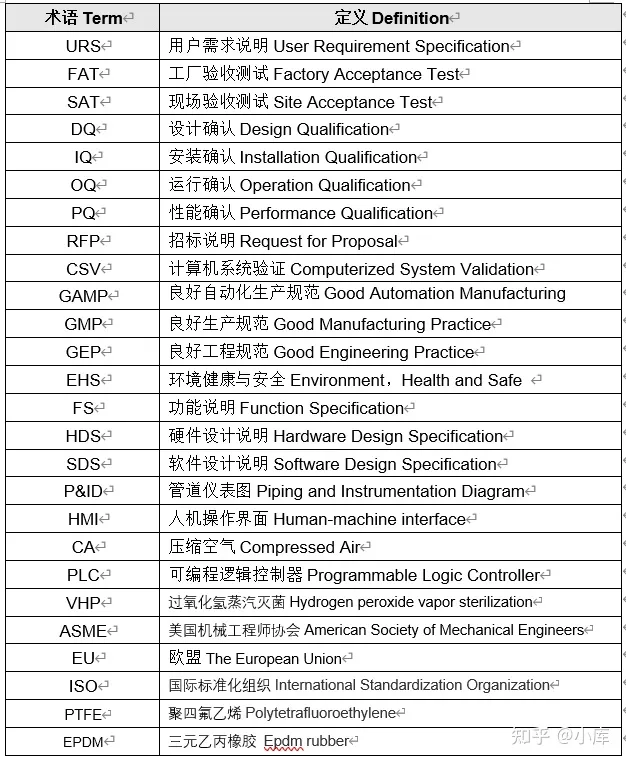
3.1无菌隔离器相关的术语
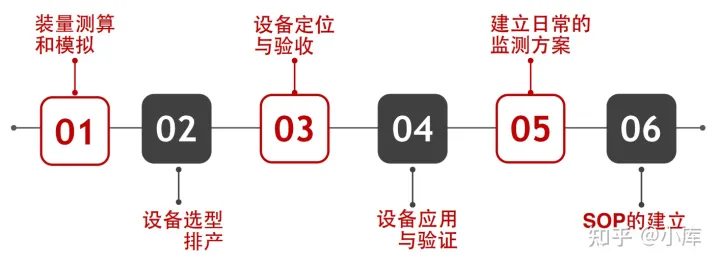
3.2从评估到使用需要做的那些事
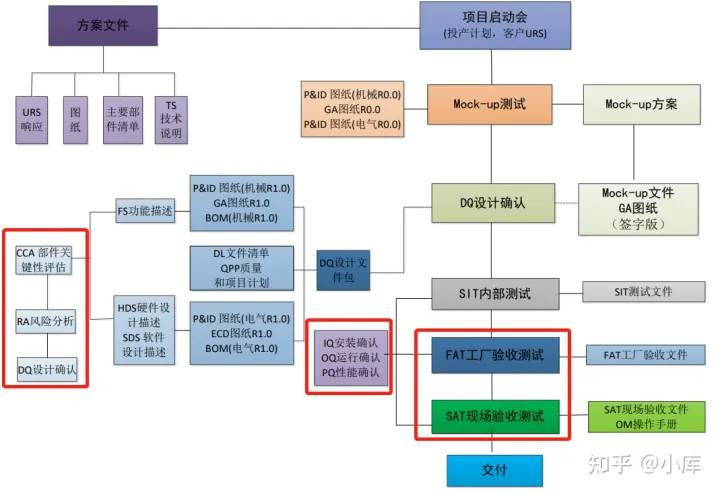
国产供应商的PPT说的很清晰,看图。
无菌检查隔离器DQ至使用前需要做的工作(仅供学习交流用)
无菌检查隔离器供应商可以做的那些事
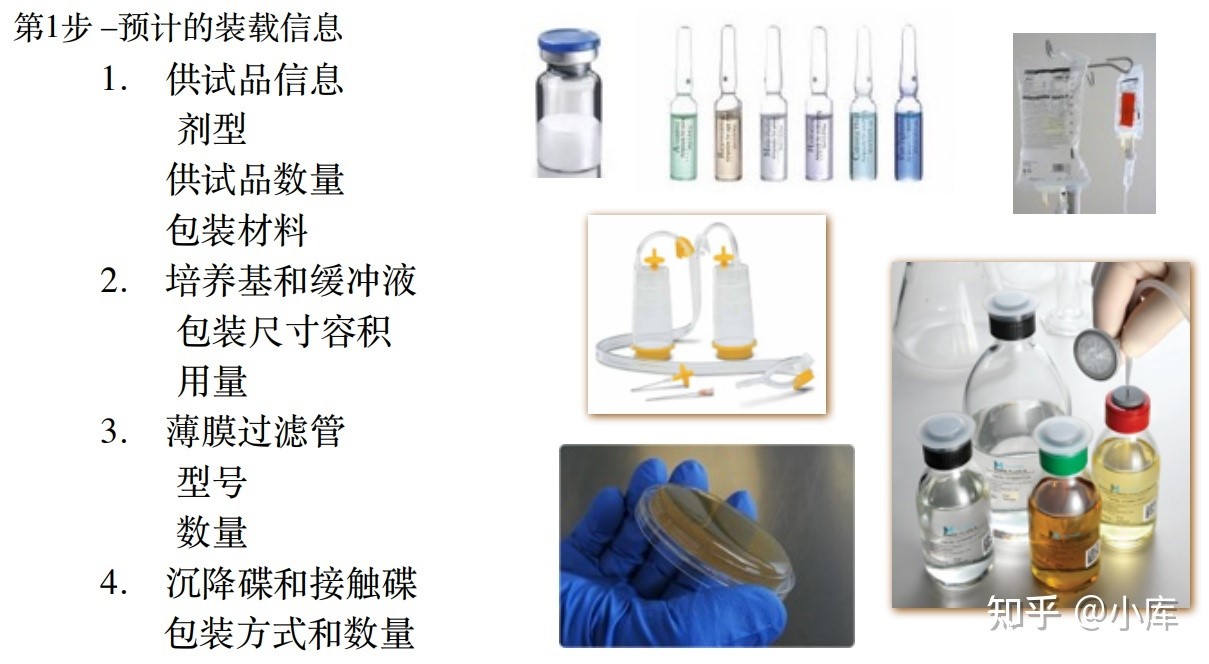
3.3预计装载信息
对于装载在我以为膜制剂、输液袋等袋装制剂是一个较大的麻烦,多是需要挂起来。其次需要强调一点就是可以采用使用杀孢子剂进行表面消毒来避免可能的假阳性,同时需要注意避免杀孢子剂残留引起假阴性。具体需要评估的装载信息见下图。
隔离器预装载信息(仅供学习交流用)
4小结
从15年隔离器大火开始,隔离器已经经过7年多的考验,很多供应商都有了较成熟的方案,现在隔离器的设计确认更多是根据自己的需求进行选配,不再是完全的设计。国产隔离器完全可以满足无菌检查需求,但是也不得不吐槽软件设计方面还是有一定的瑕疵,也许在挣钱的基础上国产供应商应该加大投入而不是一招鲜吃遍天。