



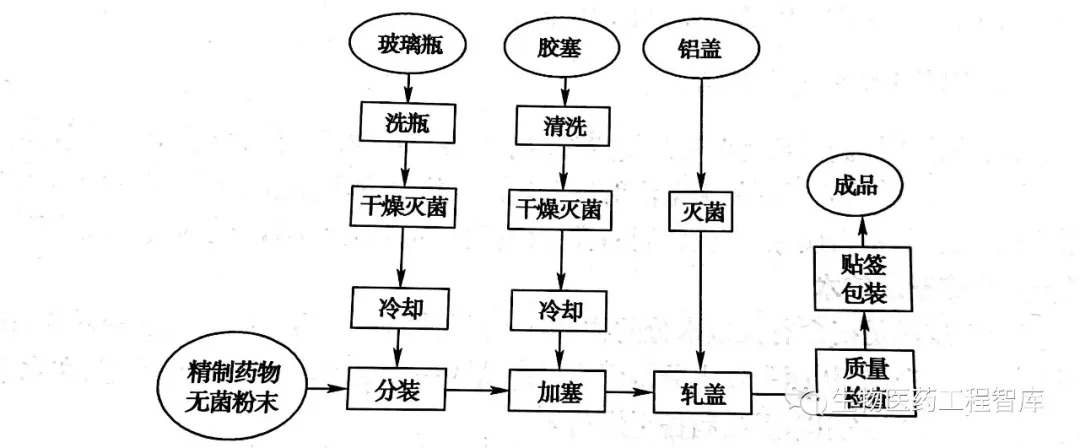
(二)基本工艺
1、原材料及容器准备 无菌原料可在无菌条件下采用结晶法或喷雾干燥法制备,必要时在无菌条件下进行粉碎、过筛等操作,制得符合分装要求的注射用无菌粉末。安瓿或玻璃瓶与胶塞的处理按注射剂的要求均需进行灭菌处理。安瓿或玻璃瓶可于180℃干热灭菌1.5小时或于250℃干热灭菌45分钟,胶塞洗净后要用硅油进行处理,再用125℃干热灭菌2.5小时或于121℃湿热,灭菌30分钟灭菌好的空瓶应在净化空气下存放,时间不应超过24小时,具体存放时间应经过验证后再确定。
2、无菌粉末的分装 分装必须在A级洁净环境中按无菌操作法进行,分装时多以容积进行定量,可用人工法或机械分装法。手工分装常采用刮板式分装器,机械分装设备有螺旋式自动分装机、直管式自动分装机和真空吸粉自动分装机等。分装机宜有局部层流装置。分装后的小瓶应立即加塞并用铝盖密封。为了避免铝屑污染产品,轧盖常与分装分开,轧盖则在另一台设备上完成。 若是安瓿,分装后应立即用火焰熔封。
3、灭菌和异物检查 对于耐热品种,可选用适宜的灭菌方法进行补充灭菌,以确保安全。 对于不耐热的品种,必须严格执行无菌操作,产品不再灭菌。异物检查一般在传送带上用目检视完成。
4、印字包装 检验合格的产品进人印字工序,目前生产均已实现机械化、自动化。
(三) 无菌分装工艺中存在的问题及解决办法
1、装量差异 主要原因是待分装无菌物料的流动性差。除此之外,吸潮和含水量、药物的晶态、粒度、比容以及机械设备性能等均会影响物料流动性,从而影响装量差异,应根据具体情况分别采取相应的措施。
2、可见异物 由于药物粉末经过一系列的处理,污染机会增加,以致可见异物不合要求。 应严格控制原料质量及其处理方法,防止污染。
3、无菌 由于产品是通过无菌操作制备的,所以生产过程中稍有不慎就有可能受到污染,而且微生物在固体粉末中的繁殖慢,不易被肉 眼观察,危险性更大。需要在经过定期监测的A级净化条件下分装。
4、吸潮变质 药物粉末吸潮,黏性增加,导致流动性下降,分装时引起装量变异大。有的药物粉末吸潮后还会引起分解变质。吸潮一般认为是由于胶塞透气性和铝盖松动所致,故要进行橡胶塞密封检测另外铝盖压紧后,必要时采用蜡封确保封口严密,此外无菌分装室的相对湿度应控制在药物的临界相对湿度以下。
注射用冷冻干燥制品
注射用冷冻干燥制品系将药物配制成无菌水溶液或均匀混悬液,分装于容器中,经冷冻干燥法除去水分,密封后得到的无菌注射粉末。凡对热敏感或在水中不稳定的药物均适用于该方法干燥。 如蛋白质、酶等生物制品:注射用重组人干扰素α2b、注射用抑肽酶等。
(一) 冷冻干燥技术
冷冻干燥技术是把含有大量水分的物料进行降温,冻结成冰点以下的固体,在真空条件下使冰直接升华,从而去除水分得到干燥产品的一种技术。凡是对热敏感、在水溶液中不稳定的药物,可以采用冻干法制备干燥粉末。
1、冷冻干燥的原理 水的三相图见下图。
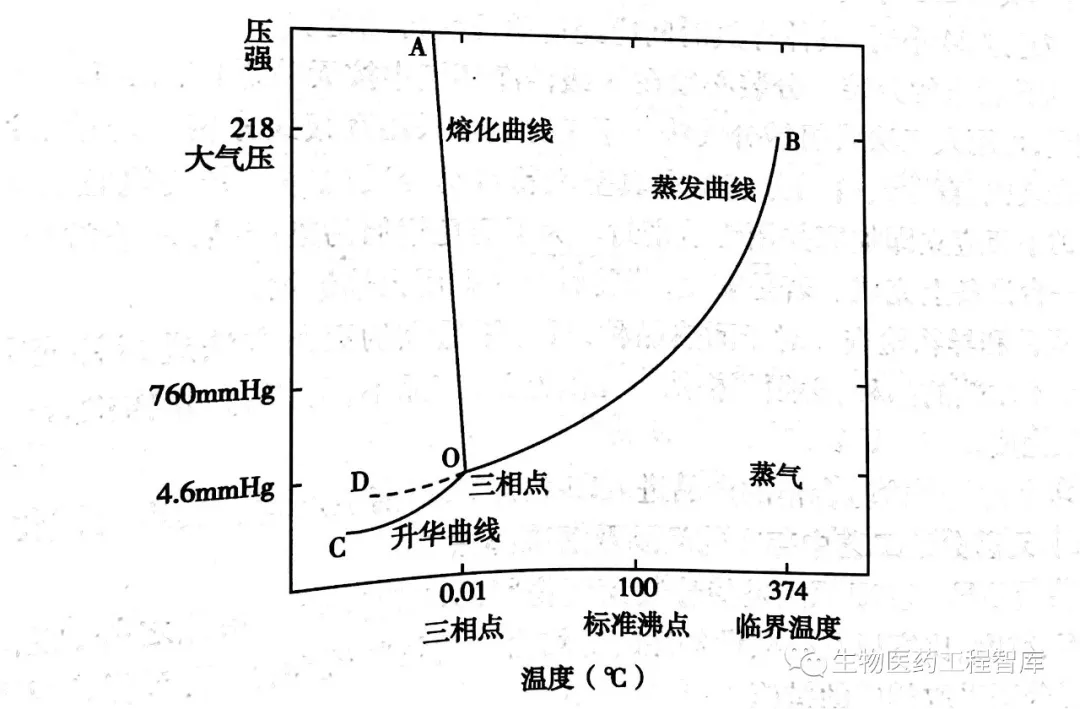
图中OA线是冰和水的平衡曲线,在此线上冰、水共存;OB线是水和水蒸气的平衡曲线,在此线上水,气共存;OC线是冰和水蒸气的平衡曲线,在此线上冰,气共存;O点是冰、水、气的平衡点。,在此温度和压力时,冰、水、气共存,即温度0.01℃,压力613.3Pa(4.6mmHg) 由图可见当压力低于613.3Pa时,无论温度如何变化,只有水的固态和气态存在,液态不存在。 固相(冰)受热时不经过液相直接变为气相;而气相遇冷时放热直接变为冰。根据平衡曲线OC,对于冰,升高温度或降低压力都可打破气固平衡,使整个系统朝着冰转变为气的方向进行,冷冻干燥就是根据这个原理进行的。
药品的冷冻干燥是指把药物溶液在低温下冻结,然后在真空条件下升华干燥,除去冰晶,待升华结束后,再进行解吸干燥,除去部分结合水的干燥方法。该过程主要可分为:药液准备、预冻、一次干燥(升华干燥)和二次干燥(解吸干燥)、密封保存等五个步骤。
升华干燥的主要目的是将冻结制品中的冰晶以升华的方式除去,也会除去一些结合水;解吸干燥的目的是将制品中残留的水除去一部分,使制品的残留水分量符合贮存的要求。药品按上述方法冻干后,可在室温下避光长期贮存,需要使用时,加灭菌注射用水或生理盐水制成溶液或混悬液,即可恢复到冻干前的状态。
2、冷冻干燥的特点 冷冻干燥因在低温、真空下干燥,具有以下突出优点:① 避免药物因高热而分解,适用于热敏性药物;② 冷冻干燥制品质地疏松多孔,体积不变,加水后迅速溶解,恢复药液原有特性;③干燥在真空下进行,药物不易氧化,同时可减少微粒的污染;④含水量低,能排除95%~99%以上的水分;⑤产品剂量准确。
缺点:冷冻干燥对溶剂的选择范围很窄,生产设备要求较高,干燥时间长,生产能耗大等。 冻干粉针制备过程中通常采用过滤除菌,不 如注射液高温灭菌效果稳定。
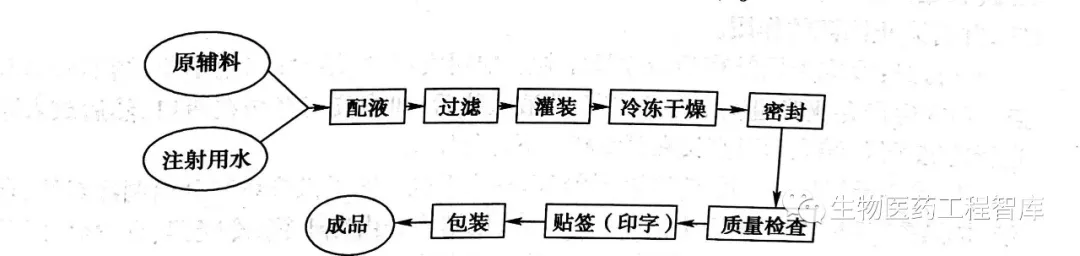
2、基本工艺 注射用冷冻干燥制品在冻干之前的操作,基本上与溶液型注射剂相同,但分装时溶液不能太厚,不超过10~15mm,以利于水分的蒸发。分装好的样品(开口)送入冷冻干燥机的干燥箱,进行预冻、升华、干燥,然后取出封口即可。
(1)预冻:制品在干燥之前必须进行预冻,如果不经预冻而直接抽真空,会使药液产生沸腾冲瓶的现象,部分药液冒出瓶外或使产品表面凹凸不平,影响产品的外观和溶解速率。通常,预冻的温度应低于产品的低共熔点10~20℃,预冻时间一般为2~3小时,有些品种需要更长时间。
预冻方法有速冻和慢冻两种方法,速冻法就是在产品进箱之前,先将冻干箱板层温度降至-30~ -50℃,再将产品进箱,速冻得到的冰晶细微,制得的产品疏松易溶。 预冻时间一般2~3小时,有些品种需要更长时间。 慢冻法是将产品直接放人冻干箱后再降低温度,慢冻得到的冰晶粗,但由于大的冰晶升华快,故慢冻可提高冻干效率。 实际工作中应根据具体情况合理选用。
新产品在确定冻干工艺时,应先获知产品的低共熔点,即在水溶液冷却过程中,冰和药物同时析晶(低共熔混合物)时的温度。在冻结与升华的过程中,制品的温度应始终低于低共熔点,否则水的冰晶体升华被液体浓缩蒸发所取代,干燥后的制品将发生萎缩、溶解速率降低等问题。
(2)升华干燥:升华干燥可根据药液性质采用一次升华法或反复预冻升华法。
1)一次升华法:先将处理好的产品溶液在冻干箱内预冻至低共熔点以下10~20℃,同时将冷凝器温度下降至-45℃以下,启动真空泵,当干燥箱内真空度达13.33Pa(0.1mmHg)以下时关闭冷冻机,通过搁置板下的加热系统缓缓加温,使产品的温度逐渐升高至约-20℃,药液中的水分不断升华,然后可将水分基本除尽。
该法适用于低共熔点为-20~-10℃的制品,而且溶液黏度不大,装量厚度在10~15mm的情况。
2)反复预冻升华法:如果制品的共熔点较低或者结构复杂、比较黏稠,如蜂蜜、蜂王浆等,这些产品在升华过程中,往往冻块软化,产生气泡,并在制品表面形成黏稠状的网状结构,从而影 响升华干燥,影响产品外观。
此时,可采用反复预冻升华法。该法的减压和加热升华过程与一次升华法相同,只是预冻过程需在共熔点以下20℃之间反复升降预冻,而不是一次降温完成。如某制品的低共熔点为-25℃,可将温度降至-45℃,然后升温到低共熔点附近(-27℃),维持30~40分钟,再降温至-40℃。如此反复,使产品结构改变,外壳由致密变为疏松,有利于水分升华,可缩短冻干周期。 此方法适用于某些共熔点较低或结构比较复杂、黏度等难于冻干的制品。
3)再干燥:当升华干燥阶段完成后,为尽可能除去残余的水,温度应继续升高至0C或室温(根据产品性质确定),并保持一段时间进行再干燥。再干燥可确保冻干制品含水量<1%,并有防止回潮的作用。
4)密封:冷冻干燥结束后应立即密封。 如用安瓿,则熔封;如用小瓶,则加胶塞及压铝盖。现在生产企业普遍使用分叉胶塞,药液灌装后,即将胶塞轻扣在瓶口,然后放入冻干室进行冷冻干燥,结束后可直接在真空状态下进行压塞。
(三)冷冻干燥中存在的问题及处理方法
[1]《药品质量生产管理规范》2010修订版